こちらのページでは熱分解・電気分解について解説しています!
酸化銀や炭酸水素ナトリウムの熱分解や、水の電気分解についてイラストや図で要点をまとめながら分かりやすく解説しています。また、テストに出やすい重要語句は赤文字で表示しています。授業の予習復習や定期テスト対策にご活用ください!
その他の理科の勉強記事もこちらから見ることができます。ぜひご覧ください!
それではさっそく見ていきましょう!
これから紹介する「分解」は、物質の化学変化のなかに分類されます。化学変化とは、物質が別の物質になる変化のことを指します。
そして、その化学変化のうち、1種類の物質が2種類以上の物質に分かれるものを分解といいます。
分解のうち加熱して分解するものを熱分解、電流を流して分解するものを電気分解といいます。(その他に、光のエネルギーによって分解する物質もあります。)
「化学変化」と「状態変化」の区別
水を冷却すると氷になった。
→ 状態変化
酸化銀を加熱すると二酸化炭素になった。
→ 化学変化
ドライアイスを加熱すると二酸化炭素になった。
→ 状態変化
炭酸水素ナトリウムを加熱すると炭酸ナトリウムになった。
→ 化学変化
ここでは、化学変化のうちの熱分解にフォーカスして見ていきます。まずは、酸化銀の熱分解について見ていきましょう。酸化銀の熱分解の実験では、図のように水上置換法を用い、ガスバーナーで酸化銀を加熱することで熱分解を行います。
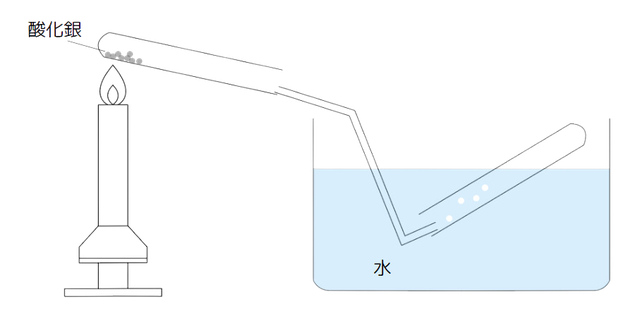
<実験の注意点>
この実験では、水上置換法を行っているビーカーの水が、酸化銀を加熱している試験管に逆流するのを防ぐため、ガスバーナーによる加熱をやめる前にガラス管を水の入ったビーカーから出す必要があります。
<実験の結果>
黒色の酸化銀を加熱すると、酸化銀は銀になり、ビーカーには気体が集まった。気体は火のついた線香を近づけると炎を出して燃えたため、酸素だということが分かった。

つづいて炭酸水素ナトリウムの熱分解について見ていきます。実験の方法は酸化銀の熱分解と同じです。
<実験の結果>
加熱後、炭酸水素ナトリウムは液体・気体・固体の3つの物質に分解した。
それぞれの物質がなにかを確認する
↓
まず、液体に関しては塩化コバルト紙が青→赤に変わったことから水であることが分かる。
次に、気体については石灰水が白く濁ったことから二酸化炭素だということが分かる。
そして最後に、炭酸水素ナトリウムから水と二酸化炭素を除いた固体=炭酸ナトリウムが残る。
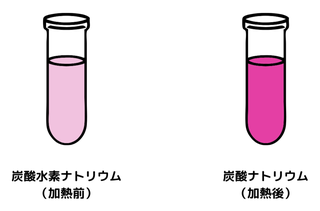
同じ量の 炭酸水素ナトリウム と 炭酸ナトリウムに、フェノールフタレイン溶液を 2滴 加えると、このイラストのようになります。このことから炭酸ナトリウム(加熱後)の方が、炭酸水素ナトリウム(加熱前)よりも強いアルカリ性を示すことが分かります。
\小・中・高校生の勉強にお悩みのある方へ/
最後に、水の電気分解について見ていきます。
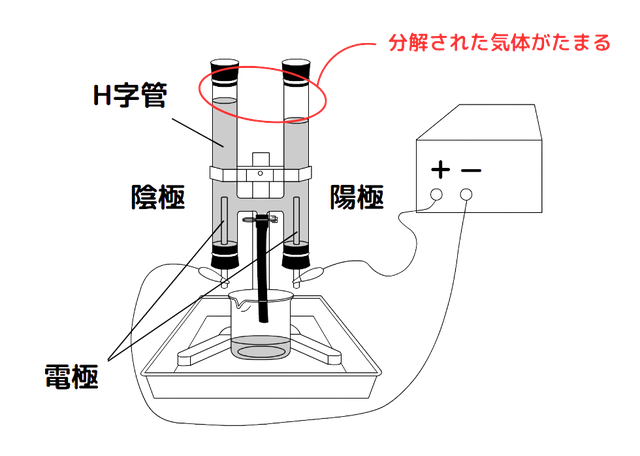
<実験の説明>
H字管の中に電気を流すための電極を入れる。
↓
ゴム栓を外してH字管の中に水を流し込み、水に電気を流す。
↓
水が分解され、それぞれの管の上部に分解された気体が溜まる。
※純粋な水は電気を通しにくいので、電気を通しやすくするために水に少量の水酸化ナトリウムを加える。
<実験の結果>
それぞれの極に集まった気体に火を近づけると、陰極側は爆発して燃え、陽極側は激しく燃えた。このことから、陽極に集まった気体は酸素で、陰極に集まった気体は水素であることが分かった。陰極側で発生した水素と陽極側で発生した酸素の量の比は2:1 で、水素は酸素の2倍発生する。
最後までお読みいただきありがとうございました。
今回は熱分解・電気分解について紹介しました。他にも理科の定期テスト対策の記事があるのでチェックしてみてください!他にも様々なお役立ち情報をご紹介しているので、ぜひご参考にしてください。質問などございましたら、お気軽にお問い合わせください!